RESUMOS
Terapias biológicas atuais e emergentes para artrite psoriásica
Apresentado por Alice B. Gottlieb, MD, FAADProfessor of Dermatology, New York Medical College, Metropolitan Hospital, New York, NY, USA
Ixequizumabe
Em dezembro de 2017, ixequizumabe foi aprovado para artrite psoriásica. O produto é administrado por injeção subcutânea e a dose recomendada é de 160 mg (duas injeções de 80 mg) na semana 0, seguidas por injeções de 80 mg a cada 4 semanas. Se os pacientes tiverem psoríase em placas moderada a grave coexistente, deve-se empregar o esquema posológico da psoríase em placas. Os pacientes não precisam usar metotrexato concomitante, já que ixequizumabe podem ser usado com ou sem metotrexato.
Os estudos clínicos de ixequizumabe demonstraram resultados significativos, que estão descritos na Tabela 1.1
Os desfechos de artrite periférica tiveram diferença significativa entre os pacientes virgens de agentes biológicos tratados com ixequizumabe: houve 57,9% de resposta pelo American College of Rheumatology 20 (ACR20) e escore Sharp total modificado (mTSS) de 0,17 no grupo do ixequizumabe, comparados a 31,1% e 0,49, respectivamente, no grupo do placebo.2 Pacientes previamente tratados com agentes biológicos também mostraram melhora, com 53% de resposta ACR20 no grupo do ixequizumabe comparados a 19% no grupo do placebo.3
Secuquinumabe
O secuquinumabe está aprovado para uso em artrite psoriásica. É administrado por injeção subcutânea e pode ou não ser iniciado com uma dose de ataque. Se administrado com dose de ataque, a posologia é de 150 mg a cada semana por 4 semanas e, em seguida, a cada 4 semanas. Sem a dose de ataque, a posologia é de 150 mg a cada 4 semanas. Se o paciente continuar apresentando artrite psoriásica ativa, a dose pode ser aumentada para 300 mg. Se os pacientes tiverem psoríase em placas moderada a grave coexistente, deve-se empregar o esquema posológico da psoríase em placas. Secuquinumabe pode ser administrado com ou sem metotrexato.4
Guselcumabe é o único medicamento que está, atualmente em fase 2 de estudos clínicos em artrite psoriásica.5 O estudo multicêntrico, randomizado, controlado por placebo irá determinar a eficácia e segurança do guselcumabe em pacientes com artrite psoriásica. O estudo, dividido em 4 partes, consiste nos seguintes períodos de tratamento:
- Período de 6 semanas de triagem
- Período de 24 semanas duplo-cego com guselcumabe ou placebo
- Período de 20 semanas de tratamento com guselcumabe
- Período de acompanhamento de 12 semanas.
O estudo incluiu uma opção de escape precoce na qual os pacientes podiam mudar para terapia aberta com ustequinumabe 45 mg ou 90 mg nas semanas 16, 20, 32 e 44 se tivessem <5% de melhora, relativamente à avaliação basal, nas contagens de articulações edemaciadas e dolorosas na semana 16. A eficácia do guselkumab será avaliada pela resposta ACR20 na semana 24.
Abatacepte é um modulador seletivo da co-estimulação de células T, cujo mecanismo de ação tem efeito no início do processo inflamatório, reduzindo a ativação das células T.6 Os resultados iniciais do estudo são relativamente promissores, com ACR20 de 39,4% e não progressão radiológica de 42,7% comparados aos respectivos resultados com placebo, ACR20 22,3% e 32,7%.7 A resposta PASI 75 parece ter sido mais pronunciada com abatacepte: 16,4% contra 10,1% do placebo.
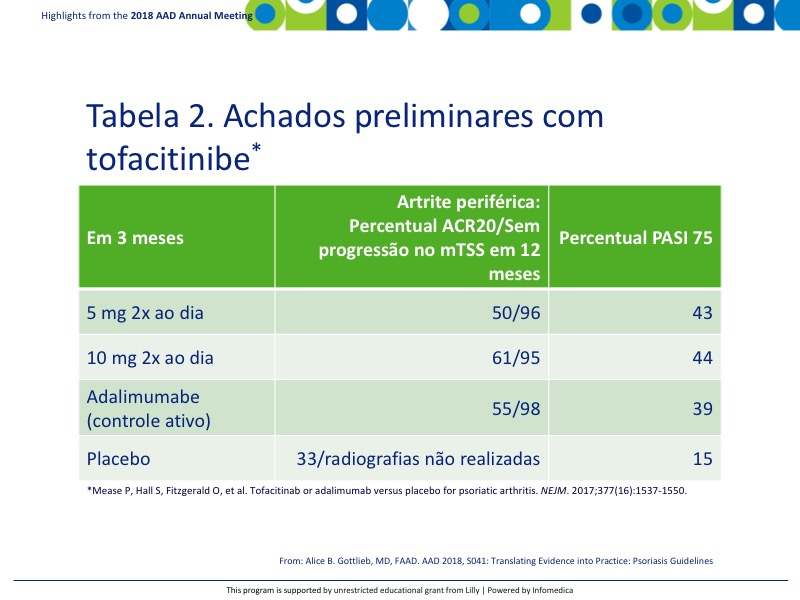
Tofacitinibe é um inibidor da quinase Janus Quinase (JAK) atualmente aprovado para artrite reumatoide. Estão em curso os estudos iniciais para determinar sua eficácia na artrite psoriásica. Os achados preliminares em pacientes virgens de agentes biológicos são descritos na Tabela 2.8
Existem vários inibidores de TNF já aprovados para artrite psoriásica, incluindo adalimumabe, etanercepte, infliximabe, golimumabe e certolizumabe. A Tabela 3 mostra os dados comparativos da análise dos desfechos primários, PASI 75 e ACR20.9
Principais mensagens
- Existem cada vez mais medicamentos disponíveis para tratar psoríase e que estão em avaliação para tratamento de artrite psoriásica.
- Embora todos os agentes biológicos analisados tenham demonstrado eficácia no tratamento de artrite periférica e manifestações cutâneas de psoríase, tofacitinibe e abatacepte não parecem proporcionar melhora da pele.


REFERÊNCIAS
Declaração de vínculo: A apresentadora declarou que presta consultoria, tem contratos como membro de conselhos consultivos e está envolvida como palestrante com as seguintes empresas: Janssen Inc, Celgene Corp, Bristol Myers Squibb Co, Beiersdorf, Inc, Abbvie, UCB, Novartis, Incyte, Lilly, Reddy Labs, Valeant, Dermira, Allergan e Sun Pharmaceutical Industries.
Redigido por: Debbie Anderson, PhD
Revisado por: Victor Desmond Mandel, MD
