RÉSUMÉS
Dermatite atopique: Nouveaux développements
Présenté par: Lawrence F. Eichenfield, MD, FAAD Professor of Dermatology and Pediatrics. University of California, San Diego. Rady Children’s Hospital, San Diego, CA, USATrente ans se sont écoulés depuis la découverte de l’activité accrue de la phosphodiestérase-4 (PDE-4) et des taux réduits d’adénosine monophosphate cyclique (AMPc) intracellulaire dans les leucocytes du sang périphérique des patients atteints de dermatite atopique (DA)1,2. Cette découverte a permis la mise au point de traitements ciblant la PDE-4 comme modalité anti-inflammatoire pour la prise en charge de la DA. On dispose à présent d’études à long terme sur les inhibiteurs de la PDE-4, comme le crisaborole topique3. Les études AD-301 et AD-302 d’une durée de 4 semaines sur l’innocuité et l’efficacité se sont déroulées à double insu, avec témoins sous excipient3. Une étude prolongée, AD-303, a suivi; elle s’est déroulée selon un protocole ouvert ne comportant qu’un seul groupe et a duré 48 semaines4.
Lors de l’étude initiale, les patients ont été assignés aléatoirement soit au crisaborole, soit à l’excipient b.i.d. pendant 28 jours. À la fin, les patients ont été inscrits à un essai prolongé où tous recevaient le crisaborole b.i.d. et étaient réévalués tous les 28 jours. Le crisaborole a donné lieu à un score ISGA statistiquement significatif d’élimination ou quasi-élimination des lésions comparativement au placebo (P < 0,001), avec une portée observée dès le jour 83. Les données d’innocuité à long terme ont démontré: fréquence faible d’effets indésirables liés au traitement (EILT), absence de différences quant aux effets indésirables au fil du temps, absence d’enjeux liés à l’accumulation et de signaux d’alarme aux plans des signes vitaux, des analyses de laboratoire, des infections ou des cancers4. Il reste encore à établir certains paramètres au sujet du crisaborole, notamment:
- Efficacité comparative
- Rapport coût-efficacité
- Effet selon les zones (visage)
- Enjeux liés à la sensation de brûlure
- Données concernant les patients de moins de 2 ans.
D’autres inhibiteurs de la PDE-4 sont actuellement à l’étude, entre autres les agents cités dans le tableau 1.
Les recherches initiales sur la crème de tapinarof (GSK2894512) chez les patients atteints de DA de modérée à grave ont donné des résultats prometteurs avec différentes doses. Des EILT ont été signalés chez 13 à 15 % des patients des groupes traités, contre 10 % des patients des groupes sous excipient. Des données concernant des EI minimes ont été rapportées pour cette étude5.
Une étude de phase 2 sur un inhibiteur JAK topique, le JTE-052, a aussi fait état de réponses similaires pour ce qui est du score EASI (Eczema Area and Severity Index) modifié par rapport aux valeurs de départ, comparativement au tacrolimus, agent actif du groupe témoin. L’étude a aussi démontré un taux beaucoup moindre de réactions au site d’application comparativement au tacrolimus6.
La voie des prostaglandines/leucotriènes est une autre avenue explorée. La voie de l’acide arachidonique est responsable de la transformation des phospholipides membranaires plasmatiques en éicosanoïdes, une classe de médiateurs inflammatoires. Alors que les leucotriènes jouent un rôle important dans la pathogenèse de l’asthme, les éicosanoïdes ont été observés en concentration élevée dans la peau des patients atteints de DA.
Le ZPL-521, un inhibiteur de la phospholipase cytosolique A2 (cPLA2) prévient la conversion des phospholipides membranaires plasmatiques en acide arachidonique, qui est l’enzyme limitant la production des éicosanoïdes7.
La prévention de la DA devrait aussi être fortement encouragée chez les nourrissons à risque élevé. L’utilisation d’émollients s’est révélée capable de réduire l’incidence de la DA chez les enfants de 6 mois [risque relatif [RR] 0,50 intervalle de confiance [IC] à 95 % 0,28-0,90] P = 0,02)8. Il a donc été suggéré qu’un traitement émollient soit administré dès la naissance comme approche faisable, sécuritaire et efficace pour la prévention de la dermatite atopique.
Le dupilumab est un puissant inhibiteur des voies IL4/IL13 (Th2) et a été approuvé pour la DA à une dose de charge de 600 mg, avec 300 mg une semaine sur deux par la suite. Les données de l’étude CHRONOS ont fait état d’une amélioration significative du score IGA (examen global par l’investigateur) et des scores EASI 75 et 90 avec le dupilumab, comparativement au placebo sur une période de 52 semaines9. Les non-répondeurs ont aussi été étudiés et s’ils n’ont pas atteint le paramètre EASI 75, ils ont néanmoins présenté des réponses jugées bonnes, très bonnes ou excellentes pour le score IGA.
Une étude est en cours pour évaluer l’innocuité à long terme du dupilumab administré à des participants pédiatriques (≥ 6 à mois à < 18 ans) souffrant de dermatite atopique10. Cette étude de phase 2a, ouverte, sur des doses croissantes chez des patients atteints de DA ayant connu un échec thérapeutique avec les corticostéroïdes topiques, portait sur l’utilisation du dupilumab chez des sujets de 6 à 11 ans et de 12 à 17 ans10. Les scores IGA pour chaque groupe ont été de 4 et 3 ou 4, respectivement. Deux niveaux de dose ont été utilisés dans chaque groupe d’âge: 2 mg/kg et 4 mg/kg. Il s’agissait d’une étude en deux volets: le volet A portant sur une dose avec un suivi de huit semaines et le volet B sur quatre doses hebdomadaires avec un suivi de huit semaines. Les études de pharmacocinétiques initiales ont montré des résultats favorables pour les deux volets de l’étude dans les deux groupes d’enfants, sans accumulation inhabituelle.
Les inhibiteurs JAK, comme le baracitinib, l’upadacitinib, le PF-04965842 et l’ASN002, ont aussi donné des résultats prometteurs chez les adultes souffrant de DA de modérée à grave.
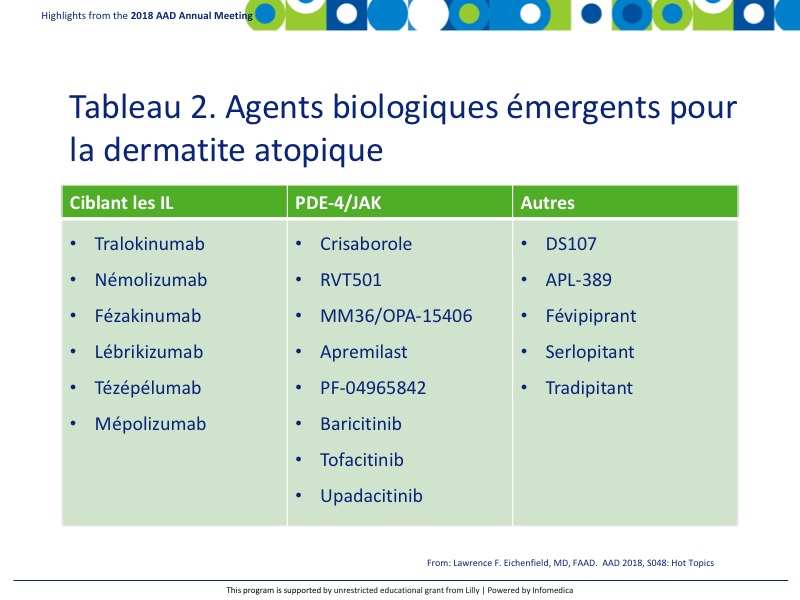
On note en amont l’émergence d’agents biologiques pour la DA dont plusieurs en sont encore au stade des essais cliniques (tableau 2). La recherche se poursuit et il est à espérer que de nouveaux traitements seront mis à la disposition des patients atteints de DA dans les prochaines années.
L’utilisation de traitements systémiques pour la DA devrait être envisagée avec circonspection. Il faut consulter les recommandations de l’International Eczema Council pour déterminer le meilleur moment et la meilleure approche lorsqu’on envisage un traitement systémique pour la DA.
Une avenue de recherche s’intéresse au microbiome comme approche pour traiter la DA. Des travaux préliminaires ont révélé la présence d’une bactérie staphylococcique coagulase-négative sur la peau qui sécrète des lantibiotiques, antimicrobiens qui agissent sur le staphylocoque doré11. La recherche dans ce domaine se poursuit et les résultats sont attendus avec impatience.
Messages clés
- Les données d’innocuité à long terme sur les inhibiteurs de la PDE-4 (plus spécifiquement sur le crisaborole) font état de résultats prometteurs et soulèvent peu d’inquiétudes.
- D’autres inhibiteurs de la PDE-4 sont actuellement à l’étude.
- La voie des prostaglandines/leucotriènes est à l’étude puisqu’il a été démontré que les patients atteints de DA présentent des taux plus élevés d’éicosanoïdes dans la peau. Le ZPL-521 fait actuellement l’objet de recherches comme approche thérapeutique possible.
- Le dupilumab et les inhibiteurs JAK gagnent en popularité parmi les agents biologiques pour le traitement de la DA. Le dupilumab a donné lieu à des réponses favorables et fait actuellement l’objet de recherches chez les enfants et les adolescents. Plusieurs autres agents biologiques sont actuellement en cours de mise au point.
- Le microbiome des patients atteints de DA serait différent. La recherche s’intéresse à une espèce staphylococcique coagulase-négative comme approche thérapeutique possible.

RÉFÉRENCES
Intérêts concurrents: Le présentateur a signalé avoir agi comme consultant ou investigateur pour Anacor/Pfizer, Cutanea, Dermavant, Genentech, Galderma Laboratories, Leo, Lilly, Matrisys, Medimedtriks, Morphosys, Novan, Novartis, Otsuka, Regeneron/Sanofi et Ortho Dermatology.
Rédigé par: Debbie Anderson, PhD
Révisé par: Victor Desmond Mandel, MD
